I
~ CANCER DU TESTICULE Andrologie (2001), 11, n ~ 2, 56-62L o c a l i s a t i o n a b e r r a n t e d e la c o n n e x i n e
43 d a n s le c a n c e r d u t e s t i c u l e .
C. ROGER1, B. MOGRABI1, D. CHEVALLIER1, J. MICHIELS2, D.
S E G R E T A I N 1 ,G. P O I N T I S 1 , P. F]~NICHEL1
I I N S E R M E M I 00-09, IFR 50, Facultd de Mddecine, 2Laboratoire d'Anatomo-pathologie, H6pital de L'Archet, Nice
RESUME
I. I N T R O D U C T I O NLa c o m m u n i c a t i o n i n t e r c e l l u l a i r e via les j o n c t i o n s gap (GJIC, p o u r ~ Gap J o n c t i o n I n t e r c e l l u l a r C o m m u n i c a t i o n -) est u n mode u b i q u i t a i r e de dialogue e n t r e les cellules. Il p a r t i c i p e a u contr61e de la prolif6ration cel- l u l a i r e . Des t r o u b l e s de l ' e x p r e s s i o n des connexines (Cx), les prot6ines t r a n s m e m b r a - n a i r e s constitutives de ces c a n a u x intercellu- laires, ont souvent 6t6 associ6s au p h 6 n o t y p e malin. Dans le tube s6minif6re, la Cx43 est exprim6e m a j o r i t a i r e m e n t p a r les cellules de Sertoli et les cellules g e r m i n a l e s basales. L'expression de la Cx43 a 6t6 6tudi6e dans u n e s6rie de 4 c a n c e r s du testicule compre- n a n t u n e prolif6ration s 6 m i n o m a t e u s e exclu- sive, ~ u n stade T1-2 NO M0. Les t r a n s c r i t s et
la
prot6ine analys6s p a r RT-PCR et Western blot, ont 6t6 retrouv6s dans t o u s l e s cas, h la taille a t t e n d u e . La p r o t 6 i n e 6tudi6e p a r i m m u n o f l u o r e s c e n c e i n d i r e c t e 6tait d61ocali- s6e au sein d u cytoplasme, n o n exprim6e ~ la m e m b r a n e , e x c l u a n t sa p a r t i c i p a t i o n ~ u n e 6ventuelle GJIC. La signification de cette localisation a b e r r a n t e de la Cx43 est discut6e dans le c a d r e des relations GJIC/tumorigen6- s e .Dans la plupart des esp~ces et quelque soit l'organe, les cellules orient6es vers la m6me fonction, sont capables de coordonner leur action, en 6changeant des informations via des jonctions communicantes ou ~, jonctions gap ,. Ces s t r u c t u r e s m e m b r a n a i r e s sp6cialis6es, p e r m e t t e n t le passage direct, de cytoplasme cytoplasme, de mol6cules de signalisation de faible poids mol6culaire (<lkDa), telles que le calcium, I'AMP cyclique, le GMP cyclique ou l'IP3, connues pour participer au contrSle du cycle cellulaire. La communication jonction- nelle intercellulaire par gap (GJIC, pour - Gap Jonction intercellular Communication , ) j o u e ainsi u n r61e de synchronisation particuli~re- m e n t important au sein du myocarde, du myo- mbtre, du systbme nerveux central ou des glandes endocrines. Elle intervient 6galement dans le contr61e de la croissance et de la diff6- rentiation cellulaires. Des perturbations de cette communication ont souvent 6t6 retrou- v6es dans les processus de prolif6ration maligne [9, 34].
Mots cl$s : cancer testiculaire, sdminome, commu- nication jonctionnelle intercellulaire par gap, sup-
presseur tumoral, connexine 43. Correspondance : P. Fdnichel, I N S E R M EM1 00-09,
IFR 50, Facultd de Mgdecine, 28 avenue de Valombrose , 06107 Nice Cedex 2
II. COMMUNICATION JONCTIONNELLE INTERCELLULAIRE PAR GAP ET
CONNEXINES
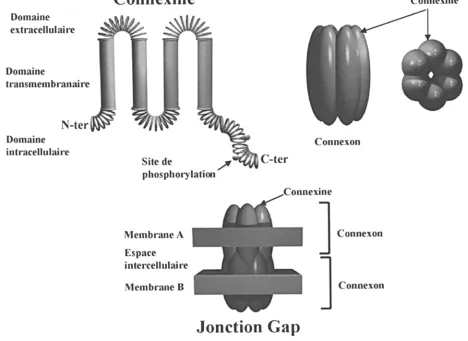
Les jonctions communicantes 6tablissent de v6ritables canaux intercellulaires regroup6s sous forme de plaques jonctionnelles membra- naires. La jonction gap est form6e par le cou- plage de deux h6mi-canaux, ou connexons, situ6s de part et d'autre des deux membranes. Les connexons sont compos6s de six connexines (Cx) identiques ou diff6rentes for- m a n t ainsi un homo- ou h6t6ro-hexam6re. Selon la composition du connexon en Cx, la perm6abilit6 du canal peut varier. Les Cx repr6sentent une famille de plus de quinze pro- t6ines t r a n s m e m b r a n a i r e s cod6es p a r des g6nes diff6rents [4] et caract6ris6es par leurs poids mol6culaires (Cx43, Cx de 43kDa). Une Cx est compos6e de quatre domaines trans- membranaires, deux boucles extracellulaires et une boucle intracellulaire et des domaines amino- et carboxy-terminaux intracytoplas- miques (Figure 1). L'extr6mit6 C-terminale poss6de des sites de phosphorylation qui sont impliqu6s dans l'ouverture ou la fermeture rapide du canal par l'interm6diaire de kinases [18, 19].
Les Cx pr6sentent une r6gulation tissu-speci- fique. La Cx43 est exprim6e ubiquitairement et est la repr6sentante de cette famille, la plus 6tudi6e h ce jour. Elle joue un r61e essentiel, en particulier, au niveau du myocarde comme le d6montrent les troubles h la naissance des sou- ris knock-out Cx43-/-, qui meurent de malfor- mations cardiaques [27]. Elle est exprim6e 6galement au niveau du foie [3], du follicule ovarien [8], du myom6tre off, sous l'effet des estrog6nes, elle coordonne les contractions ut6- rines. De plus, elle est majoritairement expri- m6e dans le testicule de rongeur [28, 1] et le testicule humain [32].
III. COMMUNICATION JONCTIONNEL. LE INTERCELLULAIRE PAR GAP
ET CANCER
Des perturbations de la communication jonc- tionnelle ont souvent 6t6 observ6es au sein de
cellules transform6es ou canc6reuses, entre elles, ou avec les cellules saines avoisinantes [9, 21, 5]. Ces troubles de la GJIC peuvent 6tre lids soit h une alt4ration de l'expression du g6ne de certaines Cx, soit h des modifications post-traductionnelles, comme des anomalies de l'6tat de phosphorylation [11, 29], ou des troubles du trafic des Cx qui ne sont alors plus localis6es ~ la membrane mais d61ocalis6es dans le cytoplasme [16]. Diff6rents promoteurs tumoraux comme le TPA sont capables d'indui- re 6galement ces anomalies [17, 26]. Les Cx sont aussi les cibles potentielles de diff6rents oncog6nes (src, ras, gay, neu) conduisant h la fermeture des canaux par hyperphosphoryla- tion du domaine C-terminal [13, 14]. P a r ailleurs, dans les diff6rents mod61es cellulaires malins off une anomalie de la GJ]C a 6t6 mise en 6vidence, la r6expression voire la surex- pression de certaines Cx par t r a n s f e r t de g~nes, conduit soit h u n ralentissement soit une normalisation de la prolif6ration cellulaire in vitro [30] et in vivo [9]. Ces observations sugg6rent que les Cx peuvent ~tre consid6r6es comme de v6ritables suppresseurs tumoraux [22].
IV. LA SPERMATOGENESE, U N P R O C E S S U S CONTROLI~
Domaine extracellulaire
Connexine
ConnexineDomaine
transmembranaire
N-ter Domaine
intracellulaire
phosphorylation
C-ter
Connexon
Membrane A
Espace intercelhflaire
Membrane B
Connexon
Connexon
Jonction Gap
Figure 1 : Reprdsentation des connexines et de la jonction Gap.
m6iose, par l'interm~diaire des Cx 43 et 37 exprim6es au niveau des cellules de la granu- losa ~quivalentes des cellules de Sertoli, et de l'ovocyte [30, 22]. De plus, l'observation des tubes s~minif~res de souris transg~niques homozygotes mfiles, pour lesquelles la r~gion codante de la Cx43 a 6t~ remplac~e respective- ment par les r~gions codantes de la Cx32 et la Cx40, a permis de constater une alt6ration de la spermatogen~se identique au syndrome des cellules de Sertoli isol6es [25]. L'ensemble de ces donn~es tendent ~ d6montrer le r61e pri- mordial de la Cx43 dans les processus de d6ve- loppement des cellules germinales, aussi bien chez le mille que chez la femelle.
A c e jour, cinq Cx ont ~t6 caract~ris~es dans le testicule de rongeur (Cx 26, 32, 33, 37 et 43). La Cx43 est la plus repr~sent6e ; elle est pr6- sente ~ la fois dans le compartiment intersti- tiel au niveau des cellules de Leydig et dans le tube s~minif'ere au niveau des cellules de Sertoli et des cellules germinales basales, sper-
matogonies et spermatocytes de premier ordre [2]. Elle est exprim~e ~ l'identique dans le tes- ticule h u m a i n normal [Defamie et coll., soumis pour publication]. Son expression varie au cours des stades de la spermatogen~se [2] et des anomalies ont 6t6 retrouv~es en cas d'alt~- rations de la spermatogen~se [1, 2].
V. E X P R E S S I O N D E L A C X 4 3 D A N S LE S E M I N O M E H U M A I N
Le cancer du testicule repr6sente le cancer le plus fr6quent de l'adulte jeune. En Europe, son incidence augmente de 2% par an (rapport du minist~re danois de l'environnement et de l'~nergie, Miljoprojekt 1995, NR290). 90% des cancers du testicule sont des s6minomes dont on distingue la forme pure (50 %). I1 s'agit alors d'une proliferation anarchique des seules cel- lules germinales indiff~renci~es.
nous a amen6 ~ 6mettre l'hypoth6se qu'une perte partielle du contr61e sertolien de la sper- matogen6se via une alt6ration de la GJIC 6ta- blie entre Sertoli/germinale, pourrait ~tre l'origine, participer ou 5tre associ6e au proces- sus de prolif6ration s6minomateuse.
Nous avons donc 6tudi6 l'6tat de la GJIC et plus particuli~rement l'expression de la Cx43 dans 4 s6minomes purs pr61ev6s chez des adultes jeunes ne pr6sentant pas d'invasion m6tastatique. A partir de tissus s6minoma- teux, congel4s ~ l'6tat frais, nous avons confir- m6 par RT-PCR, dans tous les cas, la pr6sence de transcrits de la Cx43 humaine, ~t la taille attendue de 1157 pb (Figure 2). L'analyse par Western-Blot, a r6v616 la pr6sence de la prot6i- ne ~ un poids mol6culaire de 43kDa et de ses diff4rentes formes phosphoryI6es (Figure 3). Par contre, par immunofluorescence indirecte, la prot6ine a 6t4 localis6e dans le cytoplasme et aucun signal n'a 6t6 retrouv6 au niveau mem- branaire (Figure 4). Afin de pr6ciser le trouble du trafic intracellulaire impliqu4 dans cette d61ocalisation (exocytose, endocytose, d6grada- tion), la co-localisation de la Cx43 avec des m a r q u e u r s des diff6rents c o m p a r t i m e n t s intracytoplasmiques, est a c t u e l l e m e n t en cours.
La Cx43 est donc exprim6e dans le s6minome aussi bien en terme de transcrits que de pro- t6ine, mais sa localisation est intracytoplas- mique et non membranaire, excluant donc sa participation ~ une GJIC fonctionnelle. Cette observation soul~ve au moins deux questions : quels sont les m6canismes de cette d61ocalisa- tion et est-elle la cons6quence de l'6tat trans- form6 de la cellule ? le trouble de l'adressage de la prot6ine ~ la membrane participe-t-il au pro- cessus n6oplasique ?
Le tableau 1 rapporte les cancers pour lesquels une anomalie d'expression de la Cx43 a 6t6 raise en 6vidence. Dans certains mod61es, on observe une inhibition partielle de la trans- cription, des modifications de l'6tat de phos-
phorylation de la prot6ine ou une d61ocalisa- tion de celle-ci. Une localisation aberrante a 6galement 6t6 caract6ris4e pour d'autres Cx dans des cellules tumorales [12].
I1 est possible d'envisager une mutation soma- tique portant sur une partie du g6ne codant pour un domaine impliqu6 dans l'adressage de la prot6ine ~ la membrane comme rapport6 par Krutovskikh [16]. Cependant, l'association Cancer/mutation des Cx de semble rare.
Une autre hypoth6se concernant cette d61ocali- sation cytoplasmique pourrait ~tre la pr6sence d'anomalies portant sur les prot6ines associ6es au transport membranaire. I1 est possible que certaines prot6ines, d6crites pour ~tre asso- ci6es ou participant au transport membranaire des Cx (Zonula Occludens 1, N-cadherine) [33 ;7], soient ici non exprim6es ou anormales. De plus, les diff6rents 6tats de phosphorylation des Cx observ6s dans les processus malins, pourraient 6tre /t l'origine d'une modification de leur conformation emp~chant ainsi toute liaison avec ces prot6ines associ6es.
Quant ~ la participation de la Cx43 en t a n t que facteur suppresseur tumoral, diff6rents tra- vaux sur des mod61es malins ont montr6 l'effet du r6tablissement de l'expression de la Cx43 et de la GJIC, sur la r4duction de la prolif6ration cellulaire [35]. Le r6tablissement de la GJIC, via la surexpression de la Cx43, jouerait un r61e direct sur le contr61e des diff6rentes phases du cycle cellulaire en modulant l'ex- pression des cyclines A, D1 et D2 [15, 6].
Sl
$3
F i g u r e 2 : A n a l y s e d e l'expression d e l a Cx 43 p a r R T - P C R d a n s le t e s t i c u l e h u m a i n e t d a n s 4 s ~ m i n o m e s h u m a i n s . C t r l : t e s t i c u l e h u m a i n ( 1 1 5 7 p b ) ; $ 1 - $ 4 : s ~ m i n o m e congel~ ~ l'~tat frais.
a
~,~
~,~ ,~ ~i ~i~!'
~ !~ ~ ~ i! ~ !~!~ii
I
iii~iiii~ii~iii,ii~iii~i~i~i~i~i~!i~ii~ili~iii~i!i~
~i~i~i
ili~
~!I~!II~I ~II
~I'~!I
~I!I
~iii!~iiiiiiiiiii~!i!~!~!iii~
E
C Pl
E
PO
F i g u r e 3 : A n a l y s e d e l a Cx 43 p a r Western B l o t d a n s le t e s t i c u l e h u m a i n e t d a n s le s~minome. D ~ p S t d e 15~ ~ g d e p r o t ~ i n e s . C t r l : Testicule h u m a i n ; S : S~minome. PO : f o r m e n o n - p h o s p h o r y l ~ e d e l a Cx 43. P 1 - P 2 : f o r m e s p h o s p h o r y l ~ e s d e l a Cx 43.
orgalle cerveau sein prostate enCk:~tetre humain
ov3ire humain
tiasu ou li~n~e
C6 glioma cell
normal
carcinoma
normal
P C 3 LNCaP TSU-RI ALVA-31 normal FEEC HEC.1A RL-95-2. HOSE (normal) CaOV-3 OVCAR-3 SK-OV-3 SW626 ARN
faible mveau d'ARNm de la Cx43
exprim~
non expnrrm
present nd nd prOsent pr6sent present present
forte expression
pr6sente
presente
non presente
3 formes phosphoryk~es
non presente non presente forme non phosphoryl~e forme non phosphoryl~e 3 formes phosphoryk~s forme non phosphoryk~
non presente non presente
nd nd nd nd nd Iocalisation membrane membrane membmne nd nd nd nd fonctior~lite faible fonclionneUe fonctionnelle nd
non fonctionnelle
nd nd
R6~rence
DZhu et coll ProcNat Acad.Sci. USA
voi.88 pp.1883-1887 march 1991
Sw.Lee et cog J Cell Biol
1992 Sep;118(5):1213-21
M.ZHossain at col
the prostate
38:55-59 (1999)
membrane n d S R Schlemmer at coil
membrane nd Exp Mol Palhol
nd 1999 Dec;67(3):150-63
nd i i
foncUonnelle nd nd nd nd nd
E.A Hanna et co,
Carcinogenesis 1999 Jul;20(7):1369-73
MNoguchi et coll rein humain ACHN normal non phosphoryl~e cytoplsamique Urology
NT non d6tectable non detectable 1999 Jani5311~:218-22
cellule normal nd nd nd nd
9erminale s(~linome p~sent pr6sente c~oplasrnique non fonctionnelle
T a b l e a u 1 : A n o m a l i e s d e l a Cx 43 d a n s les c a n c e r s . L e s d o n n $ e s c o n c e r n a n t les c e l l u l e s g e r m i n a l e s e t s ~ m i n o m a t e u s e s s o n t p r $ s e n t d e s d a n s ce t r a v a i l ( I N S E R M E M I 00-09).
R E F E R E N C E S
1. BATIAS C., DEFAMIE N., LABLACK A., e t a[. :
Modified expression of testicular gap junction connexin 43 during normal spermatogenic cycle and in altered spermatogenesis. Cell. Tissue Res., 1999, 298:113-121.
2. BATIAS C., SIFFROI J.P., Ft~NICHEL P., POINTIS
G., SEGRETAIN D. : Connexin43 gene expression and regulation in the roddent seminiferous epithelium. J. Histochem. Cytochem., 2000, 48:793-805.
3. BERTHOUD V.M., LEDBETTER M.L., HERTZBERG E.L., SAEZ J.C. : Connexin 43 in MDCK cells: regula- tion by a tumor-promoting phorbol ester and Ca2+. Eur. J. Cell. Biol., 1992, 57:40-50.
4. BRUZZONE R., WHITE TW, PAUL D. : Connexions with connexins: the molecular basis of direct intercel- lular signaling. Eur. J. Biochem., 1996, 238:1-27. 5. COCHAND-PRIOLLET B., RAISON D., MOLINIE V.,
GUILLAUSSEAU P.J., WASSEF M., BOUCHAUD C. : Altered gap and tight junctions in human thyroid oncocytic tumors: a study of 8 cases by freeze-fracture. Ultrastruct. Pathol., 1998, 22:413-20.
6. CHEN S.C., PELLETIER D.B., AO P., BOYNTON A.L. : Connexin 43 reverses the phenotype of transformed cells and alters cyclin-dependent kinases. Cell Growth Differ. 1995, 6:681-690.
7. GIEPMANS B.N., MOOLENAAR W.H. : The gap junc- tion protein connexin 43 interacts with the second PDZ domain of the zona occludens-1 protein. Curr. Biol., 1998, 8:931-4
8. GRANOT I., DEKEL N. : Developmental expression and regulation of the gap junction protein and trans-
cript in rat ovaries. Mol. Reprod. Dev., 1997, 47:231-9. 9. HOTZ-WAGENBLATT A., SHALLOWAY D. : Gap junctional communication and neoplastic transforma- tion. Critical Reviews in Oncogenesis, 1993, 5:541-558. 10. HANNA E.A., UMHAUER S., ROSHONG S.L., e t al. :
Gap junctional intercellular communication and connexin 43 expression in human ovarian surface epi- thelial cells and ovarian carcinomas in vivo and in vitro. Carcinogenesis, 1999, 20:1369-73.
11. HOSSAIN M.Z., JAGDALE A., PENG A.O, LECIEL C., RUO-PAN HUANG, BOYNTON A.L. : Impaired expression and postranslational processing of Connexin43 and downregulation of gap junctional communication in neoplastic human prostate cells. Prostate, 1999, 38:55-59
12. JAMIESON S., GOING J.J., D'ARCY R., GEORGE W.D. : Expression of gap junction proteins connexin 26 and connexin 43 in normal human breast and in breast tumours. J. Pathol., 1998, 184:37-43.
13. JOU Y.S., LAYHE B., MATESIC D.F, e t al. : Inhibition of gap junctional intercellular communication and malignant transformation of rat liver epithelial cells by neu oncogene. Carcinogenesis, 1995,16:311-317. 14. KANEMITSU M.Y., LOO L.W., SIMON S., LAU A.F.,
ECKHART W. : Tyrosine phosphorylation of connexin 43 by v-Src is mediated by SH2 and SH3 domain inter- actions. J. Biol. Chem., 1997, 272:22824-22831 15. KOFFLER L., ROSHONG S., KYU PARK I., et al. :
Growth inhibition in G(1) and altered expression of cyclin D1 and p27(kip-1) after forced connexin expres- sion in lung and liver carcinoma cells. J. Cell. Biochem., 2000, 79:347-354
C., et al. : Differential effect of subcellular localization of communication impairing gap junction protein connexin 43 on tumor cell growth in vivo. Oncogene. 2000, 19:505-513.
17. LABLACK A., BOURDON V., DEFAMIE N., et al. :
Ultrastructural and biochemical evidence for gap junc- tion and connexin 43 expression in a clonal Sertoli cell line: a potential model in the study of junctional com- plex formation. Cell. Tissue Res. 1998, 294:279-287. 18. LAMPE P.D., TENBROEK E.M., BURT J.M.,
KURATA W.E., JOHNSON R.G., LAU A.F. : Phosphorylation of connexin 43 on serine 368 by pro- tein kinase C regulates gap junctional communication. J. Cell. Biol., 2000, 149:1503-1512.
19. LAU A., KURATA W.E., KANEMITSU M.Y., et al. :
Regulation of connexin 43 function by activated tyroi- ne protein kinases. J. Bioenerg. Biomembr., 1999, 28:359-368.
20. LEE S.M., TOMASETTO C., SAGER R. : Positive selection of candidate tumor suppressor genes by sub- sractive hybridization. Proc. Natl. Acad. Sci. USA, 1991, 88:2825-2829.
21. LEE S.W., TOMASETTO C., PAUL D., KEYOMARSI K., SAGER R. : Transcriptional downregulation of gap- junction proteins blocks junctional communication in human mammary tumor cell lines. J. Cell. Biol., 1992, 118:1213-1221.
22. LI R., MATHER J.P. : Lindane, an inhibitor of gap junction formation, abolishes oocyte directed follicle organizing activity in vitro. Endocrinology, 1997, 138:4477-4480
23. McGINLEY D., POSALAKY Z., PORVAZNIK M, RUSSELL L. : Gap junctions between Sertoli cell and germ cells of rat seminiferous tubules. Tissue Cell., 1977, 11:741-754.
24. NOGUCHI M., NOMATA K., WATANABE J.I., SATO H., KANETAKE H., SAITO Y. : Disruption of gap junc- tional intercellular communication in human renal cancer cell lines. Urology, 1999, 53:218-222.
25. PLUM A., HALLAS G., MAGIN T., et al. : Unique and shared functions of different connexins in mice. Curr. Biol., 2000, 10:1083-1091.
26. REN P., MEHTA P.P., RUCH R.J. : Inhibition of gap junctional intercellular communication by tumor pro- moters in connexin 43 and connexin 32-expressing liver cells: cell specificity and role of protein kinase C. Carcinogenesis, 1998, 19:169-175.
27. REAUME A.G., DE SOUSA P.A., KULKARNI Set al. :
Cardiac malformation in neonatal mice lacking connexin 43. Science 1995, 267:1831-1834.
28. RISLEY M.S., TAN I.P., ROY C., SAEZ J.C. : Cell-, age- and stage-dependent distribution of connexin43 gap junctions in testes. J. Cell. Sci., 1992, 103:81-96 29. SCHLEMMER S.R., NOVOTNY D.B., KAUFMAN
D.G. : Changes in connexin 43 protein expression in human endometrial carcinoma. Exp. Mol. Pathol., 1999, 67:150-63.
30. SIMON A.M., GOODENOUGH D.A., LI E., PAUL D.L. : Female infertility in mice lacking connexin 37. Nature, 1997, 385:525-529
31. STATUTO M., AUDEBET C.H., TON OLI H., SELMI- RUBY S., ROUSSET B., MUNARI-SILEM Y. : Restoration of cell-to-cell communication in thyroid cell lines by tranfectionn with and stable expression of the connexine 32. J. Cell. Biol., 1997, 272, 24710- 24716.
32. STEGER K., TETENS F., BERGMANN M. : Expression of connexin 43 in human testis. Histochem. Cell. Biol., 1999, 112:215-220.
33. TOYOF.UKU T., YABUKI M., OTSU K., KUZUYA T., HORI M., TADA M. : Direct association of the gap junction protein connexin-43 with ZO-1 in cardiac myocytes. J. Biol. Chem. 1998, 273:12725-12731. 34. YAMASAKI H., KRUTOVSKIKH V., MESNIL M.,
TANAKA T., ZAIDAN-DABGLI M.L., OMORI Y. : Role of connexins (gap junction) genes in cell growth control and carcinogenesis. C.R. Acad. Sci. Paris, 1999, 322:1651-1659.
35. ZHU D., CAVENEY S., KIDDER G.M., NAUS C.G.C. : Transfection of C6 glioma cells with Connexin 43 cDNA: Analysis of expression, intercellular coupling, and cell proliferation. Proc. Natl. Acad. Sci USA, 1991, 88:1883-1887.
A B S T R A C T
A b e r r a n t l o c a l i z a t i o n o f c o n n e x i n 43 in testi- c u l a r c a n c e r
R O G E R C., M O G R A B I B, C H E V A L L I E R D, M I C H I E L S JF, S E G R E T A I N D, P O I N T I S G,
F E N I C H E L P
Most cells c a n c o m m u n i c a t e d i r e c t l y v i a g a p j u n c t i o n c h a n n e l s . Gap j u n c t i o n i n t e r c e l l u l a r c o m m u n i c a t i o n (GJIC) p a r t i c i p a t e s i n t h e c o n t r o l of cell p r o l i f e r a t i o n . A b n o r m a l e x p r e s - s i o n o f c o n n e x i n s (Cx), t h e c o n s t i t u t i v e pro- t e i n s of g a p j u n c t i o n s , h a s b e e n a s s o c i a t e d w i t h a t r a n s f o r m e d p h e n o t y p e . In t h e s e m i n i - f e r o u s t u b u l e s , c o n n e x i n Cx43 is p r e d o m i - n a n t l y e x p r e s s e d b y Sertoli cell a n d g e r m i n a l cell m e m b r a n e s . We s t u d i e d Cx43 e x p r e s s i o n in f o u r t e s t i c u l a r c a n c e r s (pure s e m i n o m a ) . Cx43 m R N A a n d p r o t e i n c h a r a c t e r i z e d b y RT P C R a n d Western blot w e r e f o u n d to be simi- lar to c o n t r o l s ( n o r m a l testes) in e a c h case. H o w e v e r , i m m u n o f l u o r e s c e n c e s t u d y o f Cx43 p r o t e i n i n d i c a t e d a c y t o p l a s m i c l o c a l i z a t i o n w i t h no m e m b r a n e e x p r e s s i o n , e x c l u d i n g t h e p a r t i c i p a t i o n o f Cx43 in GJIC. T h e s i g n i f i c a n - ce of t h i s a b e r r a n t l o c a l i z a t i o n w i l l b e d i s c u s - s e d in r e l a t i o n to c a r c i n o g e n e s i s .